
Leistung, die ein Ansprechen möglich macht
LYTGOBI zeigte eine objektive Ansprechrate (ORR) von 42 % bei Patienten mit zuvor behandeltem, lokal fortgeschrittenem oder metastasiertem iCCA1
ORR: 42%

2,5 Monate bis zum Ansprechen (median)
(Min-Max: 0,7 – 7,4)
Die ORR für LYTGOBI war
42 %
(95 %-KI: 32 %, 52 %)
PR: 42 %
Die Patienten hatten eine mediane Dauer des Ansprechens (mDoR) von fast 10 Monaten mit LYTGOBI1
Mediane DoR
9.7
Monate
(95 %-KI: 7.6, 17.1)


Mediane DoR
9.7
Monate
(95 %-KI: 7.6-17.1)
| Kaplan-Meier-Schätzungen der mDoR (95 %-KI) | |
|---|---|
| 3 Monate | 100 % (100, 100) |
| 6 Monate | 85.1 % (69.8, 93.1) |
| 9 Monate | 52.8 % (34.2, 68.3) |
| 12 Monate | 37.0 % (18.4, 55.7) |
FOENIX-CCA2: Zusätzliche Endpunkte
LYTGOBI unterliegt einer bedingten Zulassung.1,2
- Das bedeutet, dass weitere Nachweise zur Bestätigung der Wirksamkeit und Sicherheit dieses Arzneimittels erwartet werden.1 Die Europäische Arzneimittel-Agentur wird neue Informationen zu diesem Arzneimittel mindestens jährlich bewerten und die Zusammenfassung der Merkmale des Arzneimittels wird bei Bedarf aktualisiert.
Progressionsfreies Überleben (%) (PFS)2
Kaplan-Meier-Schätzung des PFS (N = 103)
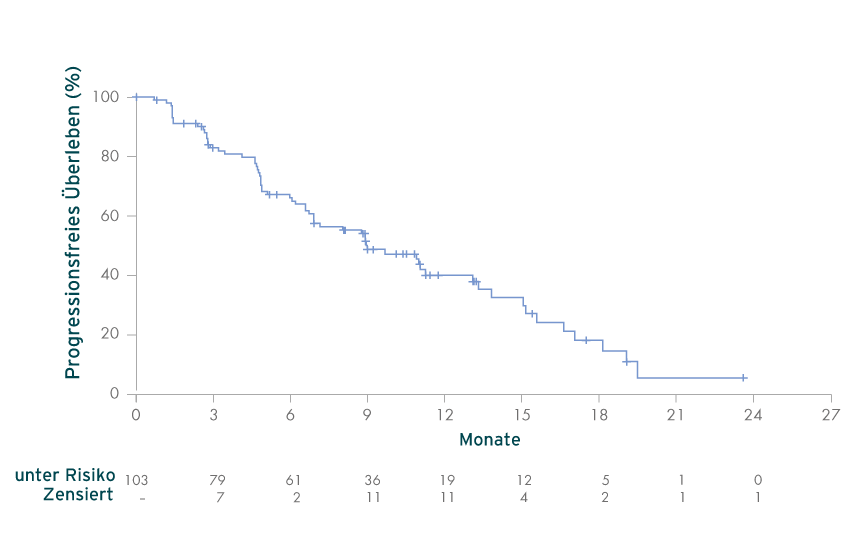
Median, 9,0 Monate (95 %-KI: 6,9, 13,1)
- Die mediane Nachbeobachtungsdauer zum Zeitpunkt des Daten-Stichtags betrug 17,1 Monate
Gesamtüberleben (OS)2
Kaplan-Meier-Schätzung des OS (N = 103)
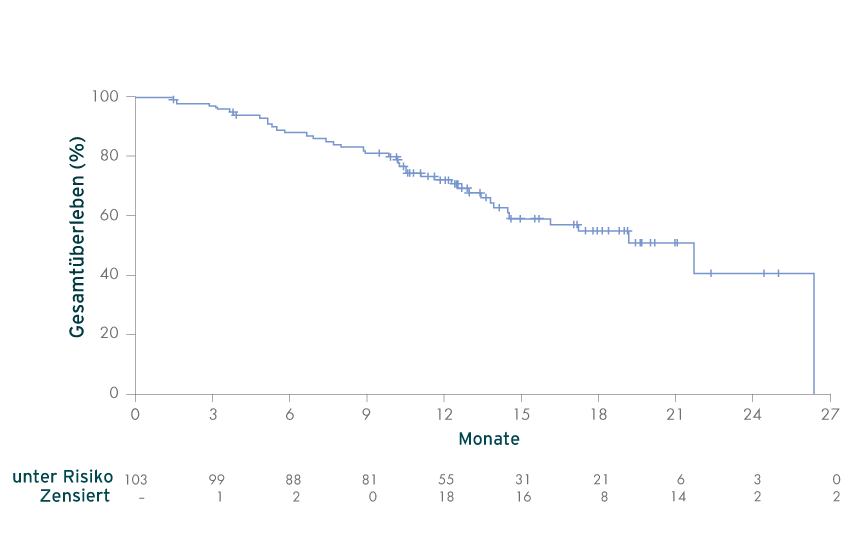
Median: 21,7 Monate (95 %-KI: 14,5, nicht erreicht)
- Zum Zeitpunkt der Analyse (1. Okt. 2020): Die mediane Nachbeobachtungsdauer betrug 17,1 Monate; die OS-Daten waren nicht ausgereift; 40 Patienten verstarben. Alle Patienten hatten die Therapie vor ihrem Tod abgebrochen, wobei der Hauptgrund für den Abbruch bei 90 % der Patienten die Krankheitsprogression war.2
- Eine reife Analyse mit einer medianen Nachbeobachtungsdauer von 25,0 Monaten (29. Mai 2021) ergab ein medianes OS von 20,0 Monaten (95 % KI: 16,4 – 24,6)2
Krankheitskontrollrate (DCR) (N = 103)2

- FOENIX-CCA2 war eine einarmige Studie2
- In diesem Setting können die DCR-Ergebnisse den natürlichen Verlauf des Cholangiokarzinoms bei einzelnen Patienten widerspiegeln, und nicht die direkte Wirkung der Behandlung
- **DCR ist die Summe aus vollständigem Ansprechen, partiellem Ansprechen und stabiler Erkrankung.
Ergänzende Ergebnisse
Ergebnisse zur Wirksamkeit bei verlängerter Nachbeobachtung
Bei einer 8 Monate nach der primären Analyse durchgeführten, nicht vorab festgelegten Nachbeobachtungsanalyse (Datenstichtag, 29. Mai 2021; mediane Nachbeobachtungsdauer, 25,0 Monate) wurde die Wirksamkeit in der gesamten Studienpopulation aufrechterhalten, mit2:
41,7 % ORR,95 %-KI: 32,1 bis51,9 % 82,5 % DCR,95 %-KI: 73,8 bis89,3 % - 9,5 Monate medianes DoR,
95 %-KI: 7,6 bis 10,4 - 8,9 Monate medianes PFS,
95 %-KI: 6,7 bis 11,0 - 20,0 Monate medianes OS,
95 %-KI: 16,4 bis 24,6
Die Daten der erweiterten Nachbeobachtung wurden nach der primären Analyse erfasst und sind deskriptiv. Die Ergebnisse sollten mit Vorsicht interpretiert werden.
DCR = Krankheitskontrollrate; DoR = Dauer des Ansprechens; iCCA = intrahepatisches Cholangiokarzinom; KI = Konfidenzintervall; Mo. = Monate; ORR = Gesamtansprechrate; OS = Gesamtüberleben; PFS = progressionsfreies Überleben; PR = partielles Ansprechen.
Referenzen:
LYTGOBI® Fachinformationen. www.lytgobi.eu/de/specialistinformation
2.Goyal L, et al. Futibatinib for FGFR2-Rearranged Intrahepatic Cholangiocarcinoma. N Engl J Med. 2023;388:228 – 239.


